
Recursos de nutrientes y su composición
1. Principios de alimentación y análisis de fertilizantes
Para conocer el valor de un ingrediente alimenticio o de un fertilizante como fuente directa o indirecta de nutrientes en dietas para peces o camarones cultivados, es necesario tener información previa sobre su valor nutricional y seguridad toxicológica. Antes de alimentar a los animales se debe hacer en primer término una descripción química, microbiológica y física del producto en cuestión.
1.1 Análisis de los alimentos
El primer paso en la evaluación química de los ingredientes que se pretenden usar en la alimentación animal, usualmente es el análisis Weende o proximal. Aquí, el material a probar es sometido a una serie de pruebas químicas relativamente simples, para determinar su contenido de humedad, proteína cruda, cenizas, lípidos, fibra cruda y carbohidratos digeribles. Una representación diagramática del esquema del método de Weende de análisis proximal de alimentos se muestra en la Figura 1.
1.1.1 Composición de nitrógeno protéico y no protéico.
El contenido de proteína cruda de un ingrediente se determina usualmente por medio del método Kjeldahl en el cual se mide el contenido de nitrógeno total en la muestra, convirtiendo luego este resultado a un valor total de proteína cruda, mediante una multiplicación por el factor empírico 6.25 (este factor de conversión se basa en la suposición de que la proteína promedio, contiene alrededor de 16% de nitrógeno por unidad de peso, aún cuando en la práctica es posible una variación entre 12 y 19% de nitrógeno entre proteínas individuales). Por ejemplo, en la Tabla 1 se muestra el rango de factores de conversión de proteína usados para convertir valores de nitrógeno a proteína cruda en diferentes materiales. Para detalles del método Kjeldahl por titulación manual vea: Munro y Fleck (1969), AOAC (1980) y MAFF (1981).
La mayor desventaja del método Kjeldahl, es que no diferencia entre nitrógeno protéico y no-protéico (NNP). Consecuentemente, aún cuando este método es generalmente satisfactorio para ingredientes alimenticios convencionales (ya que estos solo contienen pequeñas cantidades de NNP), no es el caso para proteínas
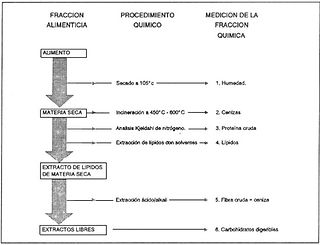
Figura 1. Método Weende de análisis proximal de alimento
microbianas unicelulares (proteína unicelular; bacterias, microalgas, levaduras) y ciertos productos animales de desecho, los cuales pueden contener cantidades considerables de NNP.
Por ejemplo, la gallinaza seca tiene un alto contenido de nitrógeno, equivalente a 28% de proteína cruda, del cual solo cerca de un tercio es verdadera proteína y el resto es NNP, principalmente en la forma de ácido úrico (Blair, 1974). En vista de la muy limitada (si no total) capacidad de los peces y camarones para utilizar NNP dietético, es esencial que ambos, la proteína verdadera y el nitrógeno no-proteico, sean determinados por separado en los nuevos ingredientes alimenticios. Para detalles de técnicas analíticas de proteína verdadera, ver Lowry et al., (1951), AOAC (1980) y MAFF (1981).
En contraste con el método Kjeldahl para estimar la calidad de la proteína, la composición de aminoácidos de un material proporciona uno de los mejores indicadores para conocer el valor nutritivo potencial. Los aminoácidos pueden ser medidos individualmente por medio de métodos microbiológicos (Barton Wright, 1972; AOAC, 1980), o por cromatografía de columna (Moore, 1963; Roach, Sanderson y Williams, 1967; Liu y Chang, 1971; Moodie et al. 1982; Williams, Hewitt y Buttery, 1982; Bos, Verbeek y Slump, 1983; AOAC, 1980). Sin embargo, se debe de recordar que los niveles de aminoácidos obtenidos de dichos análisis no indican su forma química en el alimento (ej. libre, ligado, no ligado, oxidado), o de su disponibilidad durante la digestión. Consecuentemente, la estimación de la disponibilidad de los aminoácidos en el ingrediente alimenticio es a menudo una garantía. Los métodos más comúnmente usados para evaluar la disponibilidad de aminoácidos son, la prueba de Lisina disponible (Roach, Sanderson y Williams, 1967) y la prueba de Metionina disponible (Kies, 1981; Bos, Verbeek y Slump, 1983).
1.1.2 Composición de lípidos y ácidos grasos
El contenido de lípidos en los ingredientes alimenticios es usualmente determinado por extracción en solventes como éter de petróleo (AOAC, 1980; MAFF, 1981). Otros solventes que también han sido usados en la extracción de lípidos incluyen cloroformo:metanol (Bligh y Dyer, 1959); Folch et al., 1957) y triclorofluorometano (Korn y Macedo, 1973). Aún cuando la fracción lipídica o “extracto etéreo” de ingredientes de origen animal y oleaginosas convencionales, esta compuesta predominantemente de triglicéridos, grasas y aceites, entre la PUC microbiana y ciertos materiales vegetales, alrededor de la mitad del “extracto etéreo” puede estar en forma de substancias no-glicéridos (Schultz y Oslage, 1976). Consecuentemente, ya que la mayoría de los lípidos no basados en glicéridos tienen un valor energético más bajo para peces y camarones comparado con las grasas y aceites verdaderos, es importante que el nivel de lípidos basados en glicéridos sea determinado por separado en estos productos. Entre la PUC microbiana y los alimentos animales tratados extensamente con calor (ej. alimentos expandidos con calor), se presenta una complicación adicional debido a que una porción substancial de los lípidos están presentes en una forma ligada, que requiere de hidrólisis con HCI 4N antes de la extracción con éter (Salo, 1977; Halverson y Alsting, 1981; Limsuwam y Lovell, 1985).
La composición de ácidos grasos de un lípido se determina usualmente mediante cromatografía de gases-líquidos (CGL), después de la extracción de los lípidos y su transesterificación (Morrison and Smith, 1964; Martinelli, 1967; Christie, 1973; AOAC, 1980). Debido a que los alimentos ricos en ácidos grasos poliinsaturados (AGPI) presentan una alta tendencia a sufrir daños oxidativos, se han diseñado numerosos métodos químicos para determinar el grado de oxidación o rancidez oxidativa, incluyendo contenido de ácidos grasos libres (AOAC, 1980; Ke et al., 1976; Windsor y Barlow, 1981), valor peróxido (AOAC, 1980; Pearson, 1970), valor del ácido tiobarbitúrico (Asakawa et al., 1975) y el valor de anisidina (Windsor y Barlow, 1981)
Tabla 1. Factores de conversión de proteína usados para convertir nitrógeno a proteína, entre diferentes ingredientes alimenticios¹


¹ Fuente: MAFF (1975)
² Incluye todas las carnes y pescados.
1.1.3 Contenido de fibra cruda y carbohidratos digeribles
Varias técnicas químicas están disponibles para la estimación de carbohidratos en alimentos vegetales y animales. El método más comúnmente empleado divide los carbohidratos en dos fracciones, fibra cruda y extracto libre de nitrógeno (ELN; Figura 1). La fibra cruda es el residuo orgánico insoluble, remanente después de extraer un material libre de grasa con ácido y álcali diluidos, bajo condiciones controladas. Sin embargo, el análisis de fibra en la dieta ha presentado múltiples dificultades (para una revisión de métodos analíticos, ver Southgate, Hudson y Englyst, 1978, y AOAC, 1980). La fibra cruda conocida en ocasiones como “roughage” es generalmente considerada como el componente carbohidrato no digerible de un ingrediente alimenticio o dieta. Entre los alimentos de origen vegetal, la fibra cruda se compone principalmente de varias proporciones de celulosa, hemicelulosa y lignina (esta última no es un carbohidrato, sino un compuesto aromático complejo), mientras que en productos animales, la fibra cruda se compone de varias proporciones de glucans, manans y amino azúcares.
Por otra parte, el extracto libre de nitrógeno (ELN) es una medida indirecta de los carbohidratos “solubles” o “digeribles” presentes en el alimento. Se obtiene mediante la sumatoria de los valores porcentuales determinados para la humedad, proteína cruda, lípidos, fibra cruda y ceniza, y substrayendo el total de 100. En alimentos basados en vegetales, esta fracción se compone principalmente de azúcares libres, almidón y otros carbohidratos digeribles. Sin embargo, con el desarrollo de técnicas analíticas específicas para la medición de carbohidratos individuales, es preferible medir directamente esas substancias en los alimentos (para detalles de métodos analíticos para el análisis de carbohidratos individuales, ver Somogyi, 1952; Murat y Serfaty, 1974; Harbone, 1973; AOAC, 1980; MAFF, 1981).
1.1.4 Ceniza y composición mineral
El contenido de ceniza de un alimento es el residuo inorgánico remanente, después de que la materia orgánica ha sido destruida por combustión en una mufla (AOAC, 1980; MAFF, 1981).
La composición mineral de la ceniza así obtenida, no es necesariamente la misma de como estaba originalmente presente en el material alimenticio, debido a que algunos elementos son volátiles a temperaturas superiores a 450° C (notablemente los elementos mercurio, arsénico, selenio, fósforo, cromo y cadmio; Katz, Jenniss y Mount, 1981). Consecuentemente, para análisis de minerales traza, las muestras de alimento son usualmente solubilizadas mediante una técnica de oxidación ácida previa al análisis por espectrofotometría de absorción atómica (para detalles de esos métodos analíticos, ver AOAC, 1980 y MAFF, 1981).
1.1.5 Composición de vitaminas
Las vitaminas individuales pueden ser medidas por una serie de técnicas microbianas, biológicas y químicas. Sin embargo, la mayoría de los análisis de vitaminas son bastante largos y complicados; para mayores detalles sobre técnicas analíticas, ver la revisión de Hashmi (1973) y AOAC (1980).En vista del efecto dañino potencial de esos factores antinutricionales sobre el crecimiento de peces y crustáceos, cuando estánpresentes en regímenes alimenticios completos (a niveles altos de inclusión), es importante que sea determinado su nivel y actividad en los ingredientes de origen vegetal. Para detalles de técnicas analíticas, ver, AOAC (1980); Liener (1980) y MAFF (1981).
1.1.6 Variabilidad en la composición química
Un problema que se puede encontrar con el uso de ciertos ingredientes y en particular con subproductos de plantas y animales y desperdicios de los mismos, es que su composición química puede variar considerablemente en períodos de tiempo relativamente cortos, así como de un lugar a otro (Blair, 1974; Tacon y Ferns, 1979).Una evaluación apropiada del valor nutricional potencial de un ingrediente alimenticio, debería incluir también una estimación de su variabilidad química a través de intervalos regulares de tiempo.
1.1.7 Características físicas
Además de la situación química de los nutrientes principales presentes en los alimentos, se requiere también información sobre las características físicas del producto, incluyendo color, textura, olor, tamaño de partícula y densidad.
1.1.8 Factores antinutricionales endógenos
La presencia de factores antinutricionales endógenos en los productos vegetales, es considerada como uno de los principales factores que limitan su uso en la alimentación animal. En la Figura 2 se resumen los grupos principales de factores antinutricionales presentes entre los vegetales, con ejemplos específicos en la Tabla 2. Varios de esos factores antinutricionales pueden ser encontrados también en tejidos animales; por ejemplo, el factor antivitamina Tiaminasa puede encontrarse en pescado y mariscos crudos (NCR, 1983).
1.1.9 Factores tóxicos exógenos
Los alimentos, dependiendo de su origen y procesamiento, pueden contener diferentes tóxicos exógenos incluyendo: peces venenosos, toxinas de protozoarios y algas, residuos de solventes (ocasionalmente los residuos de solventes están presentes en Los alimentos, dependiendo de su origen y procesamiento, pueden contener diferentes tóxicos exógenos incluyendo: peces venenosos, toxinas de protozoarios y algas, residuos de solventes (ocasionalmente los residuos de solventes están presentes en oleaginosas sometidas a extracción con solventes: cloruro de metileno, dicloruro de etileno, tricloroetileno, hexano, acetona, alcohol isopropílico), toxinas de hongos (ej. aflatoxinas presentes en materiales mal almacenados), toxinas bacterianas (ej. la toxina del botulismo), drogas terapéuticas (antibióticos, sulfonamidas, Nitrofuranos, ácido arsenílico), residuos de pesticidas (hidrocarbonos clorinados), compuestos organoclorados (bifeniles policlorinados), hidrocarburos (ej. n-parafinas) y contaminación por metales pesados (Friedman y Shibko, 1972; Ashley, 1972; NCR, 1983).
1.1.10 Contaminación microbiana
Entre los microbios, los alimentos basados en estiércoles y materia animal presentan una posibilidad de riesgo debido a la presencia de microorganismos contaminantes viables, incluyendo: bacterias (ej. contaminación con Salmonella en subproductos animales), hongos y virus (ej. productos de origen fecal). Para eliminar el riesgo de transmisión de enfermedades por esos productos, es esencial que sean procesados de tal forma que se asegure una completa destrucción de los microorganismos causantes de enfermedades o para reducir sus niveles a los mínimos sugeridos por los standars oficiales gubernamentales de control de alimentos (MAFF, 1973, 1976; Pierce, 1976; PAG, 1974). Para detalles de métodos analíticos ver AOAC (1980).
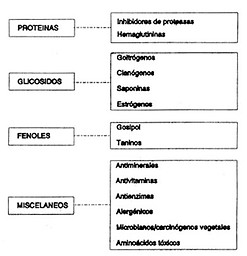
Figura 2. Clasificación de factores tóxicos endógenos presentes en forrajes vegetales de importancia agrícola (Tacón, 1985)
Tabla 2. Factores antinutricionales endógenos presentes en materiales de origen vegetal.

¹ Recopilado de los datos de Kay (1979) y Liener (1980).
Factores antinutricionales: 1. Inhibidor de proteasas; 2. Fitohemaglutininas; 3. Glucosinolato; 4. Cianógeno; 5. Ac. Fítico; 6. Saponina; 7. Taninos; 8. Factor estrogénico; 9. Latirógeno; 10. Gosipol; 11. Factor flatulento; 12. Factor antivitamina E; 13. Factor antivitamina B-1 (Tiamina); 14. Factor antivitamina A; 15. Factor antivitamina B-6 (Piridoxina); 16. Factor antivitamina D; 17. Factor antivitamina B-12; 18. Inhibidor de amilasa; 19. Inhibidor de invertasa; 20. Inhibidor de arginasa; 21. Inhibidor de colinestrasa; 22. Di-hidroxifenilalanina; 23. Mimosina; 24. Ac.graso ciclopropenoico; 25. Posiblemente contaminado con micotoxinas (Aflatoxina).
1.1.11 Certificado de análisis de ingredientes alimenticios
En todos los países, el análisis y certificación de los ingredientes para alimentación animal es normalmente controlado por un organismo regulador; por ejemplo, en el Reino Unido el análisis y certificación está controlado por “Las regulaciones de 1973 para fertilizantes e ingredientes alimenticios” del Ministerio de Agricultura, Pesquerías y Alimentos (MAFF, 1973; MAFF, 1976). Sin embargo, las regulaciones oficiales sobre ingredientes animales varían en los distintos países. En la Tabla 3 se muestra un certificado típico de análisis.
Tabla 3. Certificado oficial de análisis de MAFF (1973)

1.2 Análisis de fertilizantes
El análisis químico de fertilizantes inorgánicos (ej. compuestos minerales) y fertilizantes orgánicos (ej. estiércol y residuos vegetales), se restringe normalmente a tres clases de nutrientes; con excepción del agua se incluye:
a. Los nutrientes primarios o principales: nitrógeno (N), fosfatos (P2O5), potasio (K2O) y carbono (C).
b. Los nutrientes secundarios: azufre (S), magnesio (Mg) y calcio (Ca).
c. Los micronutrientes: fierro (Fe), cobre (Cu), zinc (Zn), manganeso (Mn), boro (B) y molibdeno (Mo).
1.2.1 Nutrientes primarios
Los niveles de nutrientes primarios en fertilizantes son usualmente expresados como porcentaje de N:P2O5:K2O. Por ejemplo, un fertilizante inorgánico etiquetado como 15:20:10 contiene 15% de nitrógeno (N), 20% de fosfato (P2O5) y 10% de potasio (K2O). Aún cuando los términos “P2O5” y “K2O” son normalmente usados para expresar los nutrientes “fosfato” y “potasio”, existe ahora la tendencia de expresar los niveles de nutrientes en los fertilizantes como el elemento solo y no como óxido. Los factores de conversión usados son:
a. Para convertir óxidos a elementos, multiplicar el valor de P2O5 por 0.4364 y el valor de K2O por 0.8302.
b. Para convertir elementos a óxidos, multiplicar el nivel de P por 2.2914 y el K por 1.2046.
El fosfato es usualmente determinado con el método del quinolinidio fosfomolibdato o por el espectrofotométrico (vanadio fosfomolibdato) (MAFF, 1973; AOAC, 1980). En esos análisis, el fosfato puede ser determinado como fósforo total y como fosfato soluble e insoluble en agua y soluble en ácido cítrico. El potasio se determina normalmente por el método del ácido perclórico o por el de cloro-platinato potásico o, en fertilizantes con menos de 20% de potasio, por el método fotométrico de flama (MAFF, 1973; AOAC, 1980). El nitrógeno por lo general se determina por el método Kjeldahl (ver sección 1.1.1) o, alternativamente en conjunto con el carbono e hidrógeno, usando un analizador automático (AOAC, 1980).
1.2.2 Nutrientes secundarios y micronutrientes
El contenido de elementos secundarios y traza de los fertilizantes, normalmente se determina usando los mismos métodos empleados con los alimentos (MAFF, 1973, 1981; AOAC, 1980; ver sección 1.1.4).
1.2.3 Variabilidad en la composición química
Al igual que en los ingredientes alimenticios, un serio problema que se puede encontrar en el uso de los fertilizantes, en particular con estiércoles y residuos vegetales, es la variación de la composición química, la cual puede ser considerable en períodos cortos de tiempo y entre estaciones del año. La evaluación de la calidad de los fertilizantes deberá incluir un análisis de variabilidad en su composición química (para límites de variación ver MAFF, 1973).
1.2.4 Contaminantes
Como en el caso de los alimentos, existe la posibilidad de que en ocasiones los fertilizantes estén contaminados con elementos minerales tóxicos, pesticidas, herbicidas, promotores de crecimiento y microorganismos patógenos (en estiércoles). Para detalles y métodos analíticos, ver AOAC (1980) y MAFF (1981).
1.2.5 Certificado de análisis de fertilizantes
El análisis y certificación de fertilizantes, al igual que en los alimentos, es normalmente controlado en todos los países por un organismo regulador (ver sección 1.1.11). En la Tabla 4 se muestra un certificado típico de análisis.
Tabla 4. Certificado Oficial de Análisis de MAFF (1973)
